|
氢
氢是一种化学元素,在宇宙诞生初期就大量存在。
在元素周期表中位于第一位,用H表示。其常规结构按粒子性来描述,可看成含有一个正价的质子与一个负价的电子组成稳定结构,两者被库仑定律束缚于氢原子内。
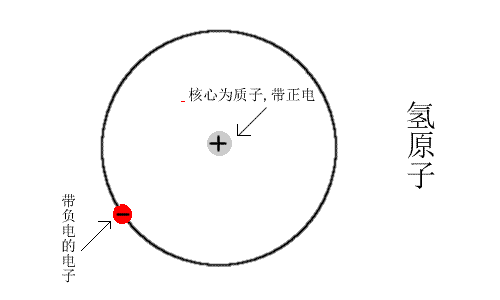
自然界中,氢只有三种同位素:氕(P)原子核内有1个质子,无中子,丰度为99.98%,这一类型最常见;氘(D)(又叫重氢),原子核内有1个质子,1个中子,丰度0.016%;氚(T)(又叫超重氢),原子核内有1个质子,2个中子,丰度0.004%。
氢元素所以被称为氢,是由其原子核内只有一个质子决定的。元素是由核内所含质子数不同进行区分的,与核内含有的中子数无关。但核内中子数的多寡,会影响到原子的稳定。
一个氢原子的实际质量为1.674×10-27千克;其直径数量级大约是10-10米,在此尺度上,氢原子内部的
真实情况要通过波粒二向性来描述。
其通常的单质形态是氢气,它无色无味无臭,由双原子分子组成,属性活跃,极易燃烧。若与氧气混合,稍有火星即会引起爆炸。氢气是最轻的气体。
氢元素在自然界中分布很广,但以单质状态存在却很少。在接近地球表面的大气里更少。其在自然界中主要以化合物的状态存在。其中最多的就是水。动植物有机体、石油、天然气、煤以及某些矿物里,也都含有大量的氢。
氢的元素符号是H,原子量是1,氢气的分子式是H2,分子量是2。
实验室里制取氢气一般用稀硫酸(H2SO4)或盐酸(HCI)做原料,通过一些活跃金属,将酸中的氢置换出来而得到游离态的氢气。实验室中常用金属锌(元素符号是Zn)来达到制氢目的。
下图是在课堂上演示制取氢气的装置示意。左面瓶内放有少量鋅粒。当从长颈漏斗加进稀硫酸后,锌粒和硫酸发生作用,很快就有氢气从锌粒表面放出,用排水集气法可以把氢气收集在集气瓶里。
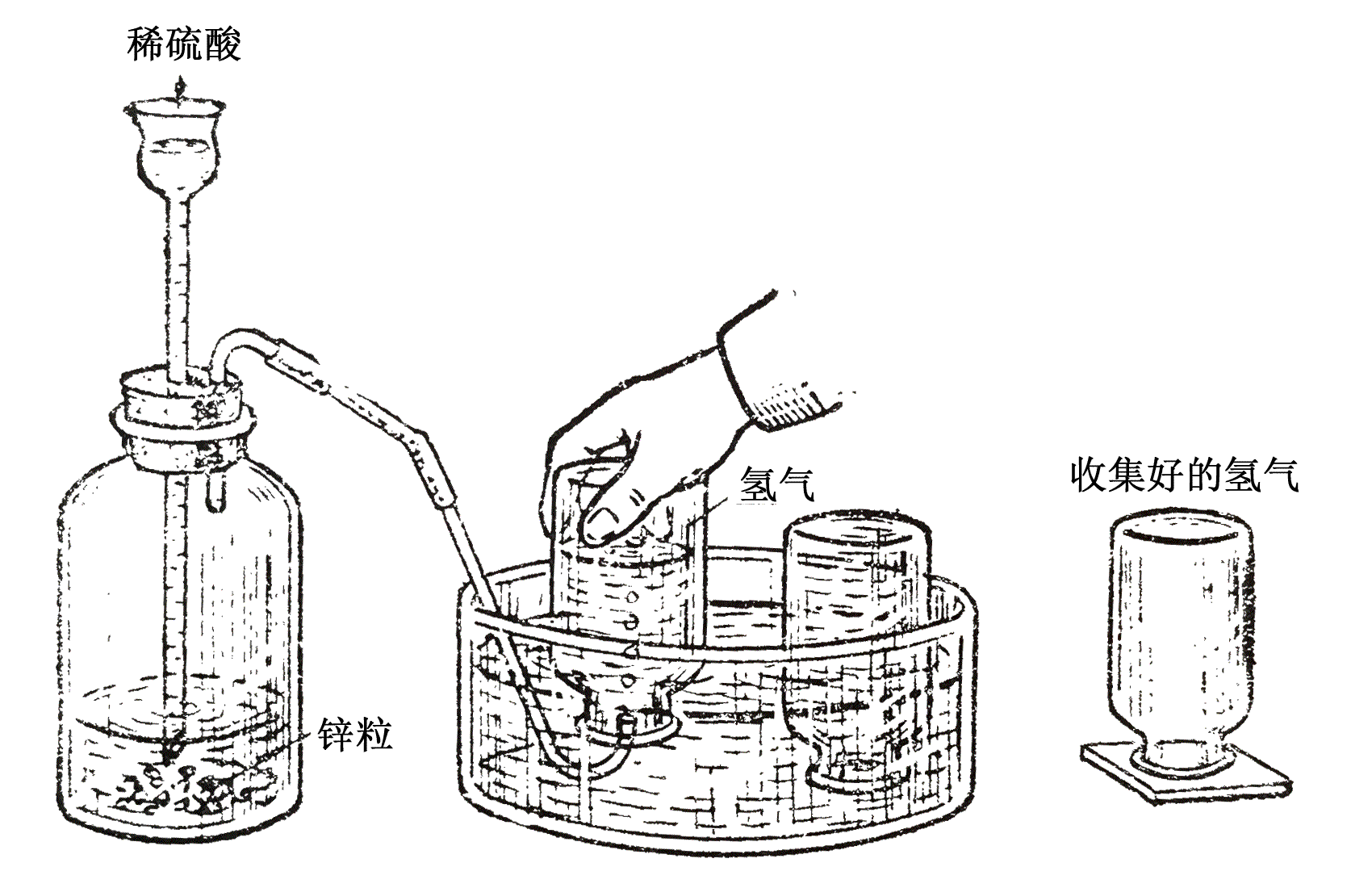
上课演示制氢装置
因为氢气比空气轻,所以集满氢气的集气瓶,要用玻片盖好瓶口,倒置在桌上。
在锌和稀硫酸的反应里,除了生成氢气外,还生成了另一种新物质叫做硫酸锌(它的分子式是ZnSO4)。锌和稀硫酸反应的化学方程式是:
|
Zn |
+ |
H2SO4 |
= |
ZnSO4 |
+ |
H2↑ |
| 锌 |
|
硫酸 |
|
硫酸锌 |
|
氢气 |
上述制氢法只能供少量制备氢气。工业上大规模制取需采用另外的方法。
因地球上含氢元素最丰富的化合物是水,所以工业制氢常用水为原料。制取方法大致有下面两类:
第一类方法是用一种单质(某些金属或非金属)在高温下和水作用,例如把水蒸气通过红热的铁屑或煤炭等物质,就能产生氢气。其本质与实验室少量制氢一样,是种置换反应。它们反应的化学方程式分别是:
3Fe + 4H2O(水蒸气) Fe3O4 + 4H2↑
Fe3O4 + 4H2↑
C + H2O(水蒸气) CO↑ + H2↑
CO↑ + H2↑
第二类方法是用电流把水分解,能高效地得到氢。这一方法,在今后的太空探索中非常重要。因为不但能得到清洁的能源,还能得到人类存活的必须品——氧气。
巩固练习
1、用足够数量的稀硫酸和13克锌作用,当锌完全作用后,能产生氢气多少克?解答
|


